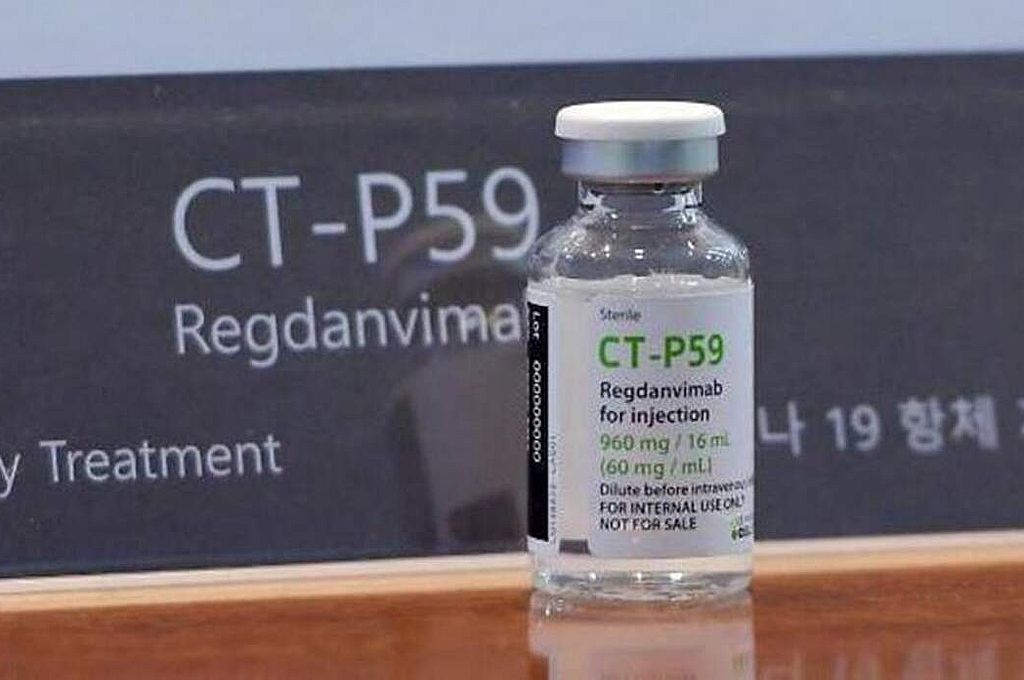
La Agencia Nacional de Vigilancia Sanitaria (Anvisa) informó en un comunicado que la dirección había aprobado “por unanimidad” la autorización “temporal de uso de emergencia del medicamento Regkirona (regdanvimabe)”, informó la agencia de noticias Sputnik.
Brasil autorizó este miércoles el uso de manera “temporal” del regdanvimabe, un nuevo medicamento contra el coronavirus indicado para pacientes que no necesitan suplemento de oxígeno, y con este ya suma cuatro fármacos para tratar casos leves del virus.
El regdanvimabe es un anticuerpo monoclonal, es decir un producto biológico producido en laboratorios y que reproduce anticuerpos que ayudan al organismo a combatir una enfermedad específica.
Este medicamento está indicado para el tratamiento de coronavirus “de leve a moderado” en pacientes adultos que no necesiten suplemento de oxígeno, pero que tengan riesgo de avanzar a la forma más grave de la enfermedad.
El nuevo medicamento contra el coronavirus será utilizado solamente en pacientes que ya hayan contraído la enfermedad
El regdanvimabe se suma a otros tres medicamentos ya aprobados por la Anvisa contra la Covid-19 para su uso en Brasil: el rendesivir, el cóctel casirivimabe+imdevimabe (Regn-CoV2), y la asociación banlanivimabe+etesevimab.
El remedio es un inyectable de uso restringido para hospitales y que debe usarse sólo después de dar positivo por SARS-CoV-2 y dentro de los siete días posteriores al inicio de los síntomas.
El principal componente del fármaco es la droga «Regdanvimab», el cual es un anticuerpo monoclonal, es decir, un producto biológico producido en laboratorios y que reproduce anticuerpos que ayudan al organismo.
En este sentido, se trata del cuarto fármaco autorizado en Brasil para el tratamiento de Covid-19 y el tercero aprobado para su uso de emergencia.
Según los estudios preliminares, la aplicación del Regkirona mostró una reducción del daño pulmonar, una disminución de la viremia (presencia de virus en la sangre) y el riesgo de hospitalización.
Según la Anvisa, esta «eficacia» llevó los organismos reguladores como la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y la Agencia Europea del Medicamento (EMA), a aprobarlos.
#Coronavirus | Brasil superó los 20 millones de contagios y concentra el 10 % de los 200 millones de casos registrados en el mundohttps://t.co/dlYSWH1ddN
— misionesonline.net (@misionesonline) August 7, 2021
El prospecto indica que el Regdanvimab debe ser utilizado para el tratamiento de Covid-19, de leve a moderado en pacientes adultos que no requieren oxígeno, con infección por SARS-CoV-2 confirmada por laboratorio y que tienen «un alto riesgo de progresión severa» de la enfermedad.
 Conmoción en Brasil: una reina de la belleza murió durante una cirugía
Conmoción en Brasil: una reina de la belleza murió durante una cirugía Jornada decisiva para Jair Bolsonaro: la Cámara de Diputados podría aprobar hoy el cambio del voto electrónico en Brasil por el impreso
Jornada decisiva para Jair Bolsonaro: la Cámara de Diputados podría aprobar hoy el cambio del voto electrónico en Brasil por el impreso Coronavirus | Brasil superó los 20 millones de contagios y concentra el 10 % de los 200 millones de casos registrados en el mundo
Coronavirus | Brasil superó los 20 millones de contagios y concentra el 10 % de los 200 millones de casos registrados en el mundo






