Algunas de las 26 personas que se estaban sometiendo al estudio Esemble, de la clínica Fundación Cardiovascular de Colombia, padecieron efectos después de la aplicación de la vacuna Johnson & Johnson. Se habían seleccionado 900 personas para los tests antes de la suspensión.
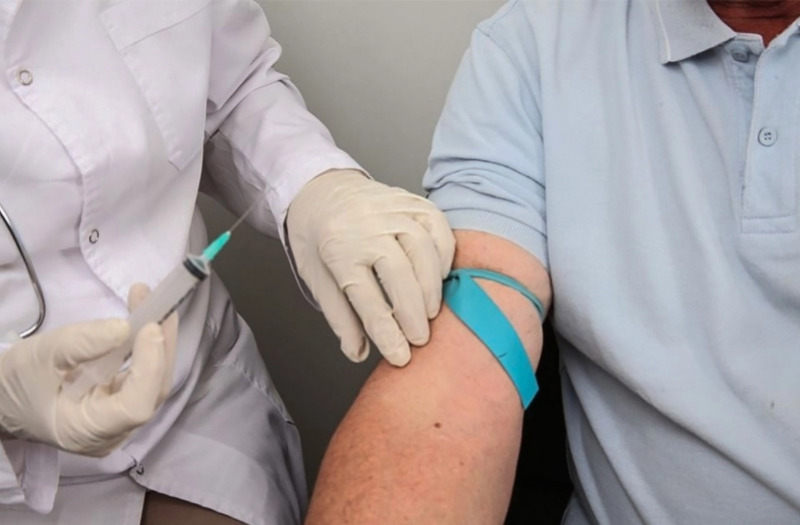
La farmacéutica estadounidense Johnson & Johnson informó recientemente que frenó de forma temporal los ensayos clínicos de su vacuna contra el coronavirus porque uno de los voluntarios se enfermó. La empresa había llegado a aplicar 26 dosis en Santander, Colombia, donde esperaban vacunar a 13 mil personas. Argentina es uno de los países donde se testea esta vacuna.
La clínica Fundación Cardiovascular de Colombia (FCV) en Floridablanca, Santander, fue uno de los centros asistenciales en los que comenzó la aplicación de las dosis el pasado miércoles 7 de octubre. Según un comunicado oficial de la clínica, el estudio Ensemble decidió suspender la vacuna contra el el SARS-CoV2 con el objetivo de evaluar su eficacia y seguridad.
En este sentido, la farmacéutica Janssen, propiedad de Johnson & Johnson, solicitó detener los estudios y no reclutar a más pacientes hasta que un comité de monitoreo y seguridad realice un análisis en el caso de la enfermedad de un participante del estudio en otro país.
El director de la Unidad de Estudios Clínicos de la FCV, Federico Arturo Silva Sieger, señaló que si bien algunos de los 26 voluntarios que se aplicaron la vacuna en Santander sufrieron síntomas como fiebre, cefalea y malestar general, “ninguno ha presentado ningún evento adverso grave ni ha requerido hospitalización”.
A pesar de esto, el experto indicó que la clínica se comprometió a contactar a cada una de las personas participantes para ponerlas en conocimiento de la problemática que se presentó.
Todo lo que tenes que saber sobre el coronavirus lo podés encontrar aquí
“Nuestro compromiso con el cuidado de las personas en investigación se mantiene de acuerdo a los exigentes estándares de la investigación y la ética, siempre dando prioridad al cuidado de las personas que participan en estos proyectos”, resaltó Silva Sieger en el comunicado.
Hasta la fecha de suspensión, en esta clínica se habían seleccionado 900 voluntarios, de los cuales 500 eran aptos para recibir las ampollas. En caso de que el estudio continúe, los voluntarios permanecerán monitoreados por dos años para verificar el comportamiento del fármaco.
En septiembre, la farmacéutica AstraZeneca, que trabaja con la Universidad de Oxford, tuvo que detener la fase III de los estudios clínicos de su vacuna debido a que uno de sus voluntarios en Reino Unido sufrió una enfermedad inesperada. No obstante, durante el mismo mes decidieron que era seguro continuar.
Fuente

 Ciudad china lanza vacuna experimental contra el coronavirus
Ciudad china lanza vacuna experimental contra el coronavirus






